Научно-исследовательский институт эпидемиологии
микробиологии и инфекционных заболеваний
 Ортга
Ортга
1. После того как я начал принимать, выписанные мне антибиотики, у меня начался понос. Почему это происходит? Появление поноса на фоне приема...
2. Можно ли при дисбактериозе кишечнике употреблять молоко? ребенку 2 года, иногда даю пить кипяченое молоко ему, и каши на молоке едим каждый день. Ребенка рвет во время еды. Кроме рвоты ничего не беспокоит: ни болей в животе, ни поноса, ни температуры нет Строгого противопоказания...
3. Может ли дисбактериоз вызвать запор у взрослого? Да, хотя при дисбактериозе...
1. Знаете ли Вы, что избавиться от глистов навсегда просто невозможно! Есть...
2. Знаете ли Вы, что при глистной инвазии происходит дефицит макро и микро...
3. Знаете ли Вы, что упущенное в детстве лечение некоторых глистных инвазий,...
Календарь событий
Разработан способ хирургического лечения больных с ахалазией кардии II-III стадии, который заключается в тотальной демускуляризации суженного отдела пищевода, селективной проксимальной ваготомии и формировании инвагинационного клапана из собственных тканей абдоминального отдела пищевода и кардии желудка. По данной методике оперированы 39 пациентов в возрасте от 23 до 62 лет с ахалазией кардии II (6) и III (33) стадий. Послеоперационных осложнений, обусловленных способом операции, не было. Период пребывания больного на койке после операции составил в среднем 6,5±1,2 сут. Данные наблюдений в сроки от 1,5 мес до 5 лет после операции свидетельствуют об удовлетворительных результатах выполненной операции не только в анатомическом, но и в функциональном аспекте, что подтверждается инструментальными методами исследования, а также изучением уровня качества жизни больных с применением шкалы GIQLI.
Ахалазия кардии (achalasia cardiac; отрицательная приставка а+chalasis — расслабление; kardia — входное отверстие желудка, греч.) — заболевание пищевода, характеризующееся нарушением рефлекторного раскрытия кардиального отверстия при глотании, нарушением перистальтики и прогрессирующим снижением тонуса тубулярного отдела пищевода. Иногда для обозначения ахалазии кардии пользуются термином «кардиоспазм», что неточно, так как при данном заболевании истинного спазма нижнего пищеводного сфинктера не происходит. Заболевание впервые описано Th. Willis в 1674 г.
Ахалазия кардии составляет от 3 до 20% всех заболеваний пищевода и встречается во всех возрастных группах, однако наиболее часто ему подвержены мужчины и женщины в возрасте от 20 до 50 лет, при этом хирургическое лечение проводится только у 10—15% больных [2—4, 6, 7].
Как правило, первыми симптомами заболевания являются преходящие признаки дисфагии, а также боли за грудиной или в эпигастральной области после акта глотания. Затем дисфагия у больных становится постоянной. Симптомы дисфагии усиливаются или уменьшаются в зависимости от эмоционального состояния. На следующем этапе болезни симптомы дисфагии и боли уменьшаются, но при этом появляется новое страдание — регургитация, носящая вначале рефлекторный характер, появляясь на высоте затруднения глотания, а в дальнейшем вызывается самим больным.
С пищеводом в ходе болезни также происходят определенные изменения. Наличие препятствия в зоне кардии ведет к его расширению и удлинению. И если в начальных стадиях заболевания емкость пищевода составляет 150—200 мл, то затем она увеличивается до 2—3 л. Кроме того, отмечаются удлинение и весьма специфическая (веретенообразная, S-образная, мешковидная) деформация пищевода [1].
И если в отношении пациентов с ахалазией кардии IV стадии вопрос о радикальном оперативном лечении с субтотальной резекцией пищевода и одномоментной его пластикой, как правило, не вызывает сомнений [2, 4], то в отношении больных co II—III стадией заболевания стараются прибегать к менее тяжелым и травматичным операциям. Наиболее распространена модификация операции, предложенной B. Heller (1913 г.), который впервые произвел внеслизистую эзофагокардиомиотомию. Сущность операции заключается в том, что из абдоминального доступа мобилизуют суженный участок пищевода и низводят его в брюшную полость. После этого мышечную оболочку в суженном сегменте пищевода продольно рассекают по передней и задней стенке до слизистой. Операция Геллера предусматривает расхождение краев рассеченных мышц пищевода, пролабирование слизистой и расширение суженного просвета пищевода. Для эффективности необходимо полное пересечение всех циркулярных мышечных волокон. Эффективность операции довольно высока — хорошие и отличные результаты достигаются в 79—91% наблюдений. Летальность, по сводным данным, составляет 0,7—1,5%. Множество рецидивов (36—50%) и отсутствие эффекта (9—14%), разнообразные осложнения в ближайшем и отдаленном периоде после операции Геллера связывают с неполным рассечением мышц кардии из-за опасности повредить слизистую пищевода. Рецидив возникает из-за развития рубца между краями пересеченных мышц с восстановлением их тонуса [5].
Нередко после операции возникает недостаточность кардии с последующим развитием рефлюкс-эзофагита и пептических стриктур пищевода, пищевода Барретта и рака пищевода. Некоторые авторы считают рефлюкс-эзофагит частым и тяжелым осложнением операции Геллера и находят его у 14—37% больных [5].
Таким образом, до настоящего времени проблема лечения больных с ахалазией кардии II—III стадии остается актуальной и требует дальнейшего исследования.
Под нашим наблюдением находились 39 пациентов с ахалазией кардии II—III стадии (см. таблицу), в том числе 16 (41,0%) мужчин и 23 (59,0%) женщины в возрасте от 23 до 62 лет (средний возраст 34,1±6,2 года).
Таблица. Распределение больных, оперированных по поводу ахалазии кардии в зависимости от пола и стадии ахалазии
| Пол | Ахалазия II
стадии | Ахалазия III
стадии | Всего больных |
| Мужской | 3 | 13 | 16 |
| Женский | 3 | 20 | 23 |
| Итого | 6 | 33 | 39 |
Распределение в зависимости от стадии заболевания проводили на основании классификации Б.В. Петровского (1962 г.):
I стадия — периодическое кратковременное затруднение прохождения пищи через нижний сфинктер из-за нарушений процесса расслабления последнего и изменений перистальтики пищевода;
II стадия — задержка пищи более продолжительна из-за стабильного спазма, что приводит к умеренному расширению пищевода над местом сужения;
III стадия — рубцовое сужение кардиального отдела со стабильным расширением вышележащих участков;
IV стадия — резко выраженный стеноз кардии с дилатацией вышележащих отделов, развитием язвенно-некротического эзофагита, периэзофагита и фиброзного медиастинита.
Длительность заболевания составила от 3 до 25 лет (в среднем 12,4±3,6 года).
Основными симптомами заболевания были дисфагия, отмечавшаяся у 36 (92,3%) пациентов, регургитация — у 32 (82,1%), боль за грудиной при глотании — у 21 (53,8%) пациентов.
Диагностику ахалазии проводили с использованием клинических и инструментальных методов (рентгенография, фиброэзофагогастроскопия, эндоскопическое и трансабдоминальное УЗИ, эзофагеальная манометрия и внутрижелудочная рН-метрия) [4], качество жизни оценивали на основании изучения гастроинтестинального индекса — GIQLI.
Всем пациентам выполняли операцию по оригинальной методике.
Перед операцией все пациенты проходили комплексное обследование, по результатам которого уточняли стадию ахалазии и определяли показания к оперативному лечению и выбирали способ его выполнения.
При эндоскопическом обследовании у больных с ахалазией кардии II стадии слизистая пищевода в верхней и средней трети была не изменена. Тонус стенки сохранялся на всем протяжении вплоть до суженного участка, где отмечалось умеренное супрастенотическое расширение. Кардия была плотно сомкнута и не раскрывалась при инсуффляции воздуха. Тубус аппарата независимо от диаметра свободно проходил в желудок, минуя суженный участок, слизистая которого также была интактна.
При ахалазии III стадии обнаруживали значительную дилатацию пищевода, в котором натощак содержались слизь и остатки пищи. Слизистая пищевода имела участки атрофии, в нижней трети была отечной, гиперемированной, местами контактно кровоточила. Кардия была сомкнута, при инсуффляции не раскрывалась, при этом тубус аппарата диаметром 11 мм проходил в желудок без усилия.
Эндоскопическое УЗИ позволяло выявить утолщение циркулярного мышечного слоя пищевода в нижней его трети (рис. 1).
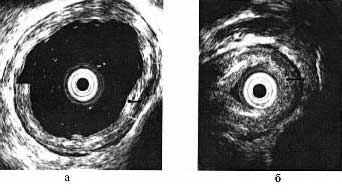
Рис. 1. УЗИ пищевода. Примечание. а - нормальная толщина мышечного слоя; б - мышечный слой утолщен до 3,5 мм в области сужения пищевода.
Толщина мышечного слоя коррелировала со стадией ахалазии и при II стадии достигала 3—4 мм, при III cтадии — 5—6 мм. При ахалазии III стадии в большинстве наблюдений отмечалась диффузная гиперэхогенность мышечного слоя в месте сужения, как признак развития соединительной ткани и рубцового изменения мышечного слоя.
При эзофагеальной манометрии у всех пациентов отмечалось повышение среднереспираторного давления в области нижнего пищеводного сфинктера более 40 мм рт.ст., снижение амплитуды перистальтических волн в теле пищевода или дистальном его участке менее 35 мм рт.ст.; расслабление нижнего пищеводного сфинктера при глотании составляло менее 60%.
По данным краткосрочной внутрижелудочной рН-метрии у 31 (79,5%) из 39 пациентов отмечалась гиперацидность на фоне базальной секреции. На фоне стимуляции доля пациентов с гиперацидностью достигала 92,3% (36 пациентов).
При рентгеноскопии регистрировалось стойкое сужение кардии на протяжении 3—4 см. Проксимальнее места сужения определялось цилиндрическое расширение пищевода на всем протяжении, достигавшее при II стадии 3—5 см, при III стадии 5—6,5 см со снижением тонуса стенки (рис. 2).
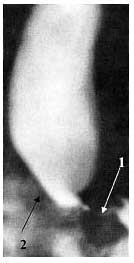
Рис. 2. Рентгенограмма пищевода при ахалазии кардии III cтадии. Примечание. 1 - участок сужения пищевода; 2 - супрастенотическое расширение
Перистальтические волны замедлены с усилением над суженной кардией и последующим ослаблением. Первичная эвакуация из пищевода происходила через 5,8±1,3 мин, (от 4,5 до 7,5 мин) небольшими и редкими порциями.
После определения показаний к выполнению хирургического вмешательства и проведения пред-операционной подготовки пациенты были оперированы.
Показаниями к проведению оперативного лечения по предлагаемой методике при ахалазии II cтадии являются:
- неэффективность или малая эффективность консервативного лечения (рецидив заболевания менее чем через 6 мес), при этом консервативное лечение включало проведение 4—6 сеансов пневматической кардиодилатации с интервалами 4—5 дней и экспозицией 3—5 мин с последующим назначением нитросорбида или коринфара (по 1 таблетке до еды) и седативных препаратов;
- отказ пациента от выполнения кардиодилатации;
- выраженность клинических симптомов (дисфагия, боль, регургитация);
- охранение перистальтической активности в стенке пищевода выше сужения по данным рентгенологического исследования и эзофагеальной манометрии.
При ахалазии III стадии операция показана при:
- неэффективности или малой эффективности консервативного лечения (рецидив заболевания менее чем через 3 мес);
- отказ пациента от выполнения кардиодилатации;
- признаки рубцового изменения мышечного слоя пищевода в месте сужения по данным эндоскопического УЗИ;
- сохранение перистальтической активности в стенке пищевода выше сужения по данным рентгенологического исследования и эзофагеальной манометрии.
Разработанная методика операции включает тотальную демускуляризацию суженного отдела пищевода с селективной проксимальной ваготомией (СПВ) и формированием инвагинационного клапана в кардиоэзофагеальной зоне и осуществляется следующим образом. Под эндотрахеальным наркозом выполняют верхнесрединную лапаротомию. После ревизии производят СПВ, мобилизацию абдоминального, внутрихиатусного отделов пищевода. В зоне кардиоэзофагеального перехода проводят тотальную демускуляризацию пищевода и кардиального отдела желудка на протяжении всего суженного участка с обязательным сохранением блуждающих нервов. Для этого выполняют поперечные циркулярные миотомные разрезы: один на 10 мм проксимальнее места сужения и другой на 10 мм дистальнее кардиоэзофагеального перехода, серозную оболочку и мышечные волокна рассекают до подслизистого слоя. Говоря о направлении миотомных разрезов, следует уточнить, что в отличие от дистального разреза, который традиционно повторяет контур кардиоэзофагеального перехода, располагаясь на 10 мм ниже его, проксимальный циркулярный разрез располагается под углом 60—70° во фронтальной плоскости (рис. 3, а).
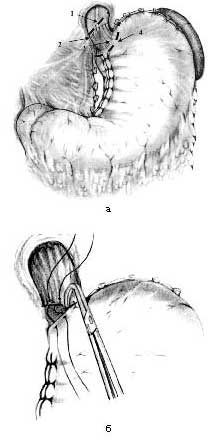
Рис. 3. Схема операции. Примечание. а - направление миотомных разрезов: 1 - циркулярный миотомный разрез на пищеводе, 2 - верхний край участка сужения, 3 - кардиоэзофагеальный переход, 4 - серозомиотомный разрез на желудке; б - при завязывании узловых швов формируется инвагинационный клапан
При таком направлении разрезов во время сопоставления тканей при сшивании формируется острый угол Гиса (близкий к анатомическому), что является еще одним составляющим компонентом антирефлюксного механизма. Без вскрытия просвета пищевода производят полное циркулярное удаление мышечного покрова, серозной и адвентициальной оболочек пищевода и желудка; после чего на нижний край мышечной оболочки пищевода и серозно-мышечную оболочку желудка накладывают узловые швы-держалки, при поочередном завязывании которых производят погружение подслизисто-слизистого футляра в просвет желудка, формируя тем самым инвагинационный арефлюксный клапан (рис. 3, б).
Формирование инвагинационного арефлюксного клапана и восстановление анатомического угла Гиса необходимо для предотвращения возникновения осложнений, связанных с забросом кислого желудочного содержимого в пищевод.
У всех 39 пациентов отмечено благоприятное течение раннего послеоперационного периода. Средняя продолжительность пребывания больного в стационаре после операции составила 6,5±1,2 сут.
В раннем послеоперационном периоде у 1 (2,6%) пациента наступил парез голосовых связок как реакция на интубацию трахеи, который был полностью купирован в первые 3 сут после операции с помощью ноотропных препаратов, витаминов группы В. Других осложнений, связанных с техникой выполнения операции, нами не наблюдалось. Энтеральное питание у всех пациентов начиналось на 3-и сутки после операции, признаков дисфагии в ответ на прием жидкой или твердой пищи не отмечалось.
Все пациенты осмотрены в сроки от 1,5 мес до 5 лет после операции.
Рецидивов заболевания не зарегистрировано. Все пациенты трудоспособного возраста вернулись к прежней работе в сроки от 12 до 16 сут. Продолжительность утраты трудоспособности составила в среднем 14,2±1,3 сут.
Фиброэзофагогастроскопия на 6-е сутки после операции: пищевод был свободно проходим, на уровне пищеводного отверстия диафрагмы имеется инвагинационный клапан, который сомкнут, свободно проходим, дефектов слизистой нет. В желудке небольшое количество жидкости. При осмотре кардиального отдела ретроградно видна характерная инвагинационная циркулярная складка высотой до 11—15 мм с умеренной гиперемией, отеком, дефектов слизистой не определялось.
Данные осмотра через 3 года и 5 лет после операции: слизистая пищевода на всем протяжении не изменена, кардиальный отдел сомкнут, при его ретроградном осмотре видна характерная инвагинационная циркулярная складка высотой до 15 мм в виде конуса, охватывающая плотно тубус эндоскопа — бледно-розовая, блестящая, без видимых дефектов. Гастроэзофагеальных рефлюксов не зафиксировано ни в одном наблюдении (рис. 4).
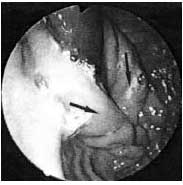
Рис. 4. Арефлюксный клапан (указан стрелками). Примечание. Эндофотография (ретроградный осмотр)
Рентгеноскопия в отдаленном периоде (от 1 года до 5 лет): поступление контрастной массы в желудок через пищеводно-кардиальный переход порционное. Расширения пищевода нет. Кардия раскрывается до 15—17 мм, полностью смыкаясь у всех обследованных. Газовый пузырь в желудке выражен хорошо у всех пациентов. При обследовании больных в положении Тренделенбурга заброса контрастной массы в пищевод не отмечено (рис. 5).
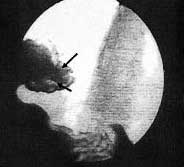
Рис. 5. Рентгенограмма через 5 лет после операции в положении Тренделенбурга на животе. Примечание. Гастроэзофагеальный рефлюкс отсутствует. Стрелками указан контур клапана
Изучение качества жизни до и после операции по шкале GIQLI, показало значительное улучшение состояния пациентов, особенно в отдаленные сроки. Так, если до операции средний балл по шкале GIQLI составлял 89,6±6,9, то уже через год после коррекции — 121,9±5,2. При этом положительный результат операции отмечался по всем пяти шкалам: общее субъективное восприятие своего здоровья; психическое и физическое состояние; социальное и ролевое функционирование (рис. 6).
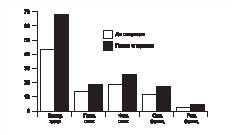
Рис. 6. Динамика качества жизни после оперативного лечения по поводу ахалазии кардии II-III стадии
Таким образом, разработанный способ хирургического лечения ахалазии кардии II—III стадии, заключающийся в тотальной демускуляризации суженного участка пищевода без вскрытия просвета органа, исключает возможность возникновения одного из наиболее тяжелых осложнений — несостоятельности анастомоза; сформированный инвагинационный клапан сохраняет органическую и функциональную состоятельность, обеспечивая профилактику рецидива и высокий уровень качества жизни больных в отдаленном послеоперационном периоде.
26.04.2018
Соғлиқни сақлаш вазирлиги: ЭМЛАШ ҚАМРОВИ 99,5 ФОИЗГА ЕТКАЗИЛДИ
Шу йилнинг 24 апрель куни “Пойтахт” бизнес марказининг мажлислар залида Соғлиқни сақлаш вазирлиги томонидан...
15.03.2018
Тиббиётни бутунлай ўзгартирадиган 11 та технологик инновация
Биз тиббиёт ва соғлиқни сақлаш соҳасидаги катта ўзгаришлар остонасида турибмиз. Улар албатта рўй беради...
27.02.2018
Ўзбекистонлик олимлар ўзак ҳужайра трансплантациясини ўзлаштириб, уни муваффақиятли йўлга қўйди
Республика Гематология ва қон қуйиш илмий текшириш институти олимлари жаҳон тиббиётининг илғор йўналиши...






