
Республики Узбекистан
Перинатальный
Центр
-
Контакты:
Адрес: ул. Дж. Абидовой 223
Телефон: +99871 260-28-80
«Ксофлюза»: японское суперлекарство для лечения гриппа
- Японская «Сионоги и Ко» (Shionogi & Co.) получила одобрение Министерства труда, здравоохранения и социального обеспечения Японии на инновационный препарат «Ксофлюза» (Xofluza, балоксавира марбоксил), предназначенный для лечения вируса гриппа типа A и B. Впрочем, в продажу он поступит не ранее мая, поскольку не закрыт вопрос со стоимостью медикамента.
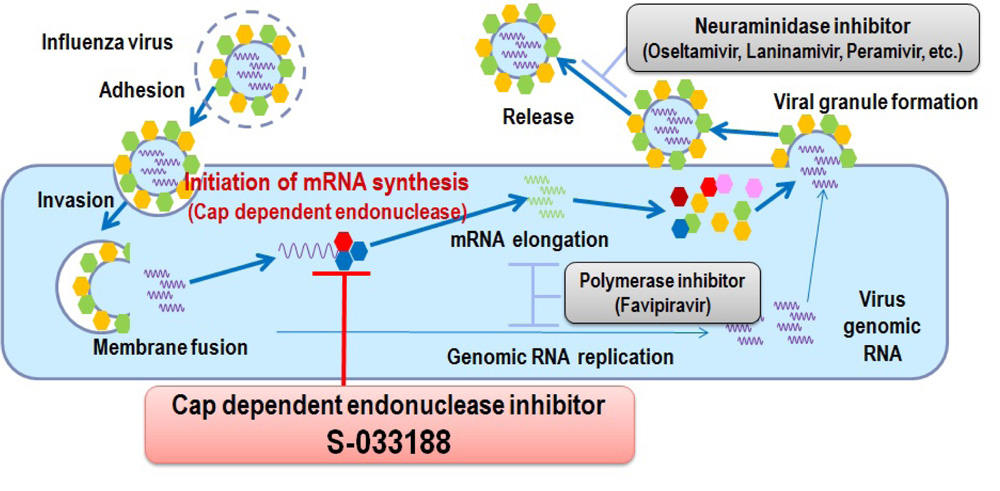
- Балоксавира марбоксил (baloxavir marboxil, S-033188) — ингибитор кэп-зависимой эндонуклеазы, механизм действия которого полностью отличается от всех существующих лекарственных средств. В отличие от ингибиторов нейраминидазы, таких как «Тамифлю» (Tamiflu, осельтамивир), «Реленза» (Relenza, занамавир), «Рапиваб» (Rapivab, перамивир) и «Инавир» (Inavir, ланинамивир), которые препятствуют откреплению вирионов от поверхности инфицированных клеток, тем самым ограничивая распространение инфекции по организму, балоксавира марбоксил подавляет репликацию вируса гриппа. Молекула ингибирует инициацию синтеза мРНК — первый этап пролиферации вируса после его попадания в клетку, в результате становится невозможным образовывать протеины, необходимые для формирования вирусной частицы.
- Как утверждается, достаточно однократно принять «Ксофлюза» (дозировка зависит от возраста и/или веса), и этого будет достаточно, чтобы уничтожить вирус гриппа за 24 часа. Согласно оценкам ВОЗ, грипп ответственен за 290–650 тыс. смертельных исходов ежегодно.
Подробности
Клинические исследования CAPSTONE-1 фазы III охватили 1436 человек, у которых был диагностирован грипп без осложнений. Критерии включения: подмышечная температура минимум 38 °C, не менее одного респираторного и одного системного симптома, прошло не более 48 часов после начала проявления заболевания. Испытуемым в возрасте 20–64 лет назначали либо единственную однократную дозу 40 или 80 мг балоксавира марбоксила (в зависимости от массы тела: <80 или ≥80 кг), либо 75 мг осельтамивира дважды в сутки на протяжении пяти дней, либо плацебо. Участники в возрасте 12–19 лет получали 40 или 80 мг балоксавира марбоксила либо плацебо.
- Группа балоксавира марбоксила продемонстрировала существенно более короткое медианное время, потребовавшееся на устранение симптомов (TTAS), если сравнивать с плацебо: 53,7 против 80,2 часов (p<0,0001). Показатель TTAS для групп балоксавира марбоксила и осельтамивира оказался схожим. Речь идет о совокупности всех семи симптомов гриппа, включающих кашель, боль в горле, головную боль, заложенность носа, лихорадку или озноб, боль в мышцах или суставах, усталость.
- Зафиксировано значительное улучшение важной вирусологической конечной точки: в первый, второй и четвертый день после начала лечения процент пациентов с позитивным титром вируса гриппа или определяемым наличием его РНК оказался гораздо ниже в группе «Ксофлюза», нежели в группах осельтамивира и плацебо. Так, по прошествии 24 часов после начала терапии вирусный титр в среднем снизился на 4,4; 1,2 и 2,5 log10TCID50/мл соответственно (p<0,0001).
- Медианное время до прекращения вирусовыделения вышло на 24, 72 и 96 часов — соответственно в группах балоксавира марбоксила, осельтамивира и плацебо (p<0,0001).
- Отмечено ускоренное исчезновение лихорадочного состояния: медианное время составило 24,5 часов против 42,0 часов в группе плацебо (p<0,0001).
- Время возвращения к состоянию здоровья до инфицирования вирусом гриппа — 129,2 против 168,8 часов в группе плацебо. Разница — почти 40 часов.
«Сионоги и Ко» утверждает, что «Ксофлюза» проявляет антивирусную активность in vitro и in vivo против вируса гриппа A и B, а также птичьего гриппа H5N1 и H7N9. Заявлено, что одновременное назначение балоксавира марбоксила и какого-либо из ингибиторов нейраминидазы определяет синергичную противовирусную активность in vitro.
Продолжаются клинические испытания CAPSTONE-2 фазы III, проверяющие «Ксофлюза» на пациентах с высоким риском осложнений гриппа. К таким лицам относятся в том числе страдающие астмой или хроническим легочным заболеванием, морбидным ожирением, диабетики, с ослабленной иммунной системой, старше 65 лет и прочие категории.
«Ксофлюза» разрабатывался «Сионоги и Ко» в партнерстве с «Рош» (Roche), с которой в феврале 2016 года было заключено лицензионное соглашение. Оно и понятно, ведь швейцарский фармацевтический гигант лишился патентной защиты на свой «Тамифлю», и потому отчаянно нуждается в нехудшей замене этого бестселлера.
Тем временем «Янссен» (Janssen), входящая в состав «Джонсон энд Джонсон» (Johnson & Johnson), вышла на завершающие этапы клинических испытаний экспериментального пимодивира (pimodivir) — монотерапевтически и в комбинации с осельтамивиром. Пимодивир, лицензированный у «Вертекс фармасьютикалс» (Vertex Pharmaceuticals) в 2014 году, представляет собой ингибитор субъединицы PB2 в составе полимеразного комплекса вируса гриппа A. Механизм его действия завязан на таргетировании альтернативной части процесса вирусной репликации. Пимодивир способен успешно подавлять грипп A, который приобрел устойчивость к уже существующим антивирусным препаратам с иным механизмом действия.
Против вируса гриппа также применяются амантадин и римантадин, блокаторы протонного канала M2. В России и Китае продвигается совершенно древний ингибитор слияния (фузии) «Арбидол» (Arbidol, умифеновир), запатентованный еще в 1974 году: молекула ингибирует поверхностный вирусный белок гемагглютинин и подавляет слияние вирусной липидной оболочки с клеточными мембранами, тем самым предотвращая проникновение вируса внутрь клетки.
Источник: mosmedpreparaty.ru






