Виды вакцин и пути их введения
Виды вакцин
Вакцины состоят из действующего начала — специфического антигена; консерванта для сохранения стерильности (в неживых вакцинах); стабилизатора, или протектора, для повышения сроков сохраняемости антигена; неспецифического активатора (адъюванта), или полимерного носителя, для повышения иммуногенности антигена (в химических, молекулярных вакцинах). Специфические антигены, содержащиеся в вакцине, в ответ на введение в организм вызывают развитие иммунологических реакций, обеспечивающих устойчивость организма к патогенным микроорганизмам. В качестве антигенов при конструировании вакцин используют: живые ослабленные (аттенуированные) микроорганизмы; неживые (инактивированные, убитые) цельные микробные клетки или вирусные частицы; извлеченные из микроорганизмов сложные антигенные структуры (протективные антигены); продукты жизнедеятельности микроорганизмов — вторичные метаболиты (например, токсины, молекулярные протективные антигены): антигены, полученные путем химического синтеза или биосинтеза с применением методов генетической инженерии.
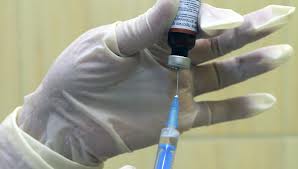
В соответствии с природой специфического антигена вакцины делят на живые, неживые и комбинированные (как живые, так и неживые микроорганизмы и их отдельные антигены). Живые вакцины получают из дивергентных (естественных) штаммов микроорганизмов, обладающих ослабленной вирулентностью для человека, но содержащих полноценный набор антигенов (например, вирус коровьей оспы), и из искусственных (аттенуированных) штаммов микроорганизмов. К живым вакцинам можно отнести также векторные вакцины, полученные генно-инженерным способом и представляющие собой вакцинный штамм, несущий ген чужеродного антигена (например, вирус оспенной вакцины со встроенным антигеном вируса гепатита В).
Неживые вакцинах подразделяют на молекулярные (химические) и корпускулярные. Молекулярные вакцины конструируют на основе специфических протективных антигенов, находящихся в молекулярном виде и полученных путем биосинтеза или химического синтеза. К этим вакцинам можно отнести также анатоксины, которые представляют собой обезвреженные формалином молекулы токсинов, образуемых микробной клеткой (дифтерийный, столбнячный, ботулинический и др.). Корпускулярные вакцины получают из цельных микроорганизмов, инактивированных физическими (тепло, ультрафиолетовое и другие излучения) или химическими (фенол, спирт) методами (корпускулярные, вирусные и бактериальные вакцины), или из субклеточных над-молекулярных антигенных структур, извлеченных из микроорганизмов (субвирионные вакцины, сплит-вакцины, вакцины из сложных антигенных комплексов).
Молекулярные антигены, или сложные протективные антигены бактерий и вирусов, используют для получения синтетических и полусинтетических вакцин, представляющих собой комплекс из специфического антигена, полимерного носителя и адъюванта. Из отдельных вакцин (моновакцин), предназначенных для иммунизации против одной инфекции, готовят сложные препараты, состоящие из нескольких моновакцин. Такие ассоциированные вакцины, или поливакцины, поливалентные вакцины обеспечивают иммунитет одновременно против нескольких инфекций. Примером может служить ассоциированная АКДС-вакцина, в состав которой входят адсорбированные дифтерийный и столбнячный анатоксины и коклюшный корпускулярный антиген. Существует также семейство полианатоксинов: ботулинический пентаанатоксин, противогангренозный тетраанатоксин, дифтерийно-столбнячный дианатоксин. Для профилактики полиомиелита применяют единый поливалентный препарат, состоящий из аттенуироваиных штаммов I, II, III серотипов (сероваров) вируса полиомиелита.
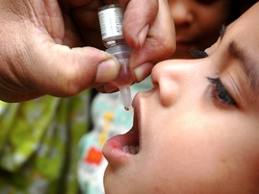
Насчитывается около 30 вакцинных препаратов, применяемых с целью профилактики инфекционных болезней; примерно половина из них живые, остальные инактивированные. Среди живых вакцин выделяют бактерийные — сибиреязвенную, чумную, туляремийную, туберкулезную, против Ку-лихорадки; вирусные — оспенную, коревую, гриппозную, полиомиелитную, паротитную, против желтой лихорадки, краснухи. Из неживых вакцин применяют коклюшную, дизентерийную, брюшнотифозную, холерную, герпетическую, сыпнотифозную, против клещевого энцефалита, геморрагических лихорадок и другие, а также анатоксины — дифтерийный, столбнячный, ботулинический, газовой гангрены.
Основным свойством вакцин является создание активного поствакцинального иммунитета, который по своему характеру и конечному эффекту соответствует постинфекционному иммунитету, иногда отличаясь от него лишь количественно. Вакцинальный процесс при введении живых вакцин сводится к размножению и генерализации аттенуированного штамма в организме привитого и вовлечению в процесс иммунной системы. Хотя по характеру поствакцинальных реакций при введении живых вакцин вакцинальный процесс и напоминает инфекционный, однако он отличается от него своим доброкачественным течением.
Вакцины при введении в организм вызывают ответную иммунную реакцию, которая в зависимости от природы иммунитета и свойств антигена может носить выраженный гуморальный, клеточный или клеточно-гуморальный характер.
Эффективность применения вакцин определяется иммунологической реактивностью, зависящей от генетических и фенотипических особенностей организма, от качества антигена, дозы, кратности и интервала между прививками. Поэтому для каждой вакцины разрабатывают схему вакцинации.
В зависимости от способа применения вакцины делят на инъекционные, пероральные и ингаляционные. В соответствии с этим им придается соответствующая лекарственная форма: для инъекций применяют исходные жидкие или регидратированные из сухого состояния вакцины; пероральные вакцины — в виде таблеток, конфет (драже) или капсул; для ингаляций используют сухие (пылевые или регидратированные) вакцины.
Вакцины будущего
-
Генно-инженерные вакцины. В геном живых аттенуированных вирусов, бактерий, дрожжей или клеток эукариотов встраивается ген, кодирующий образование протективного антигена того возбудителя, против которого направлена вакцина.
-
Синтетические пептидные вакцины. Могут содержать различные эпитопы, способные формировать иммунитет к разным видам инфекций. Отличаются высокой степенью стандартности, безопасны, однако слабо иммуногенны и требуют применения эффективных адъювантов.
-
ДНК-вакцины — вакцины из плазмидных ДНК, кодирующих протективные антигены возбудителей инфекционных заболеваний. Такая ДНК при введении в организм проникает в ядро клетки, длительное время существует вне хромосом без репликации, транскрибируется и экспрессирует соответствующие антигены, вызывающие в организме формирование T- и B-клеточного иммунитета.
-
Антиидиотипические вакцины. Антиидиотипические антитела являются зеркальным отражением антигена и поэтому способны вызывать образование антител и цитотоксических клеток, реагирующих с антигеном. Вакцины на основе антиидиотипических антител безопасны, так как идиотипы являются естественными эндогенными регуляторами иммунного ответа.
-
Вакцины, содержащие продукты генов гистосовместимости. Каждой инфекции соответствует свой набор антигенов гистосовместимости, отвечающий за высокий уровень иммунного ответа. Отсутствие на клетках таких антигенов является одной из основных генетических причин слабой иммунной реакции. Введение в организм молекул гистосовместимости, несущих пептиды, соответствующие эпитопам инфекционных агентов, будет способствовать усилению иммунитета.
-
Растительные вакцины. Продемонстрировано, что в листьях трансгенного табака могут нарабатываться белки инфекционных вирусов. После очистки такие белки можно использовать как компоненты вакцин. Немаловажное значение имеет высокая экономичность растительных вакцин и возможность их применения с пищей.
-
Мукозальные вакцины. Один из подходов к созданию таких вакцин заключается в разработке средств, препятствующих колонизации возбудителей инфекций на поверхности слизистых оболочек. Основу таких вакцин может составить белок адгезии на концах бактериальных пилей, с помощью которых бактерии прикрепляются к поверхности слизистой.
Пути введения вакцин
Внутримышечный путь введения вакцин
Наиболее предпочтительный путь для введения вакцин. Хорошее кровоснабжение мышц гарантирует и максимальную скорость выработки иммунитета, и максимальную его интенсивность, поскольку большее число иммунных клеток имеет возможность «познакомиться» с вакцинными антигенами. Удаленность мышц от кожного покрова обеспечивает меньшее число побочных реакций, которые в случае внутримышечного введения сводятся лишь к некоторому дискомфорту при активных движениях в мышцах в течение 1-2 дней после вакцинации.
Место в 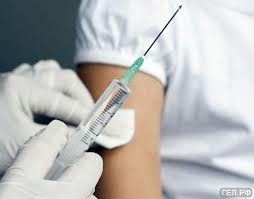 ведения: Вводить вакцины в ягодичную область крайне не рекомендуется. Во-первых, иглы шприц-доз большинства импортных вакцин недостаточно длинны (15 мм) для того, чтобы достичь ягодичной мышцы, в то время, как известно, и у детей, и у взрослых кожно-жировой слой может иметь значительную толщину. Если вакцина вводится в ягодичную область, то она по сути вводится подкожно. Следует также помнить о том, что любая инъекция в ягодичную область сопровождается определенным риском повреждения седалищного нерва у людей с анатомическими особенностями его прохождения в мышцах.
ведения: Вводить вакцины в ягодичную область крайне не рекомендуется. Во-первых, иглы шприц-доз большинства импортных вакцин недостаточно длинны (15 мм) для того, чтобы достичь ягодичной мышцы, в то время, как известно, и у детей, и у взрослых кожно-жировой слой может иметь значительную толщину. Если вакцина вводится в ягодичную область, то она по сути вводится подкожно. Следует также помнить о том, что любая инъекция в ягодичную область сопровождается определенным риском повреждения седалищного нерва у людей с анатомическими особенностями его прохождения в мышцах.
Предпочтительным местом введения вакцин у детей до 3 лет является передне-боковая поверхность бедра в средней его трети. Это объясняется тем, что мышечная масса в этом месте значительна при том, что подкожно-жировой слой развит слабее, чем в ягодичной области (особенно у детей, которые еще не ходят).
У детей старше двух лет и взрослых предпочтительным местом введения вакцин является дельтовидная мышца (мышечное утолщение в верхней части плеча, над головкой плечевой кости), в связи с небольшой толщиной кожного покрова и достаточной мышечной массой для всасывания 0,5-1,0 мл вакцинного препарата. У детей младших возрастов это место введения вакцин не используется в связи с недостаточным развитием мышечной массы и большей болезненностью.
Техника вакцинации: Независимо от выбранного места введения вакцины внутримышечная инъекция должна быть произведена перпенди кулярно, то есть под углом 90 градусов к поверхности кожи. При введении вакцины в дельтовидную мышцу инъекция производится строго сбоку, положение шприца должно быть строго горизонтальным.
Так называемая техника Z-track состоит в том, что перед инъекцией кожа сдвигается в одном из направлений и отпускается после того, как игла будет выведена. С одной стороны – прохождение иглы через натянутую кожу менее болезненно, с другой стороны, за счет смещения канала, вакцина как бы «запечатывается» в мышце.
Преимущества: хорошее всасывание вакцины и, как следствие, высокая иммуногенность и скорость выработки иммунитета. Меньшее число местных побочных реакций. Точность введенной дозы (по сравнению с внутрикожным и пероральным способом введения).
Недостатки: Субъективное восприятие детьми младшего возраста внутримышечных инъекций несколько хуже, чем при других способах вакцинации.
Пероральный (т.е. через рот)
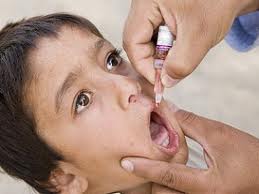 Классическим примером пероральной вакцины является ОПВ – живая полиомиелитная вакцина. Обычно таким образом вводятся живые вакцины, защищающие от кишечных инфекций (полиомиелит, брюшной тиф). Впрочем, сейчас разрабатываются пероральные вакцины, которые будут защищать не только от кишечных инфекций – вакцина против ВИЧ-инфекции на бактериальном носителе (сальмонелла).
Классическим примером пероральной вакцины является ОПВ – живая полиомиелитная вакцина. Обычно таким образом вводятся живые вакцины, защищающие от кишечных инфекций (полиомиелит, брюшной тиф). Впрочем, сейчас разрабатываются пероральные вакцины, которые будут защищать не только от кишечных инфекций – вакцина против ВИЧ-инфекции на бактериальном носителе (сальмонелла).
Техника пероральной вакцинации: несколько капель вакцины закапываются в рот. Если вакцина имеет неприятный вкус, ее закапывают либо на кусочек сахара, либо печенья.
Преимущества такого пути введения вакцины очевидны: для такой вакцинации не требуется специального образования и подготовки, простота метода, его быстрота, экономия на привлечении квалифицированного персонала.
Недостатками перорального введения вакцин следует считать разлив вакцины, неточность дозировки вакцины (часть препарата выводится с калом, не сработав), экономические потери на необходимости повторных введений вакцины и ее разливе.
Внутрикожный и накожный
Классическим примером вакцины, предназначенной для внутрикожного введения, является БЦЖ. Примерами вакцин с внутрикожным введением являются живая туляремийная вакцина и вакцина против натуральной оспы. Как правило, внутрикожно вводятся живые бактериальные вакцины, распространение микробов из которых по всему организму крайне нежелательно. Однако в последнее время, внутрикожное введение вакцин в ряде стран стало использоваться в целях экономии вакцины (для такой вакцинации требуется меньший объем вакцины) – так, к примеру, в некоторых странах прививают против бешенства. И ВОЗ, идя навстречу пожеланиям медработников, разработало рекомендации по внутрикожному введению антирабических вакцин. Для других вакцин, кроме названных, внутрикожный путь введения пока не рекомендован.
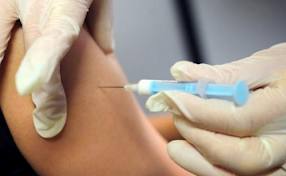
Техника: Традиционным местом для накожного введения вакцин является либо плечо (над дельтовидной мышцей), либо предплечье – середина между запястьем и локтевым сгибом. Для внутрикожного введения должны использоваться специальные шприцы со специальными, тонкими иглами. Иголочку вводят вверх срезом, практически параллельно поверхности кожи, оттягивая кожу вверх. При этом необходимо убедиться, что игла не проникла под кожу. О правильности введения будет свидетельствовать образование специфической «лимонной корочки» в месте введения – белесый оттенок кожи с характерными углублениями на месте выхода протоков кожных желез. Если «лимонная корочка» не образуется во время введения, значит вакцина вводится неверно.
Преимущества: Низкая антигенная нагрузка, относительная безболезненность.
Недостатки: Довольно сложная техника вакцинации, требующая специальной подготовки. Возможность неправильно ввести вакцину, что может привести к поствакцинальным осложнениям.
Подкожный путь введения вакцин
Довольно традиционный путь введения вакцин и других иммунобиологических препаратов на территории бывшего СССР, хорошо известный всем уколами «под лопатку» (так вводятся гангренозные и стрептококковые анатоксины). В целом этот путь подходит для живых и инактивированных вакцин, хотя предпочтительно использовать его именно для живых (корь-паротит-краснуха, желтая лихорадка и др.). В связи с тем, при подкожном введении несколько снижается иммуногенность и скорость выработки иммунного ответа, этот путь введения крайне нежелателен для введения вакцин против бешенства и вирусного гепатита В.
Подкожный путь введения вакцин желателен для пациентов с расстройствами свертывания крови – риск кровотечений у таких пациентов после подкожной инъекции значительно ниже, чем при внутримышечном введении.
Техника: Местом вакцинации могут быть как плечо (боковая поверхность середины между плечевым и локтевым суставами), так и передне-боковая поверхность средней трети бедра. Указательным и большим пальцами кожа берется в складку и, под небольшим углом, игла вводится под кожу. Если подкожный слой у пациента выражен значительно, формирование складки не критично.
Преимущества: Сравнительная простота техники, незначительно меньшая болезненность (что несущественно у детей) по сравнению с внутримышечной инъекцией. В отличие от внутрикожного введения, можно ввести больший объем вакцины или другого иммунобиологического препарата. Точность введенной дозы (по сравнению с внутрикожным и пероральным способом введения).
Недостатки: «Депонирование» вакцины и как следствие – меньшая скорость выработки иммунитета и его интенсивность при введении инактивированных вакцин. Большее число местных реакций - покраснений и уплотнений в месте введения.
Аэрозольный, интраназальный (т.е. через нос)
Считается, что подобный путь введения вакцин улучшает иммунитет во входных воротах воздушно-капельных инфекций (корь, грипп, краснуха) за счет создания иммунологического барьера на слизистых оболочках. В то же время, созданный таким образом иммунитет не является стойким, и в то же время общий (т.н. системный) иммунитет может оказаться недостаточным для борьбы с уже проникшими через барьер на слизистых в организм бактериями и вирусами.
Типичным примером интраназальной вакцины является одна из отечественных противогриппозных вакцин.
Техника аэрозольной вакцинации: несколько капель вакцины закапываются в нос либо распыляются в носовых ходах с помощью специального устройства.
Преимущества такого пути введения вакцины очевидны: как и для пероральной вакцинации, для аэрозольного введения не требуется специального образования и подготовки; такая вакцинация создает отличный иммунитет на слизистых оболочках верхних дыхательных путей.
Недостатками перорального введения вакцин следует считать существенный разлив вакцины, потери вакцины (часть препарата попадает в желудок), недостаточный общий иммунитет.