



Онлайн услуги
-
Опишите подробнее процедуру подписки на журнал
Подписка на журнал осуществляется через АК «Matbuot tarqatuvchi», ОАО “Узбекистон почтаси” и их филиалы, а та...
-
Можно ли скачать журнал в PDF формате?
Да, можно...
Чтобы высказать Ваши предложения, замечания или задать вопрос , пожалуйста, заполните приведенную ниже форму.Подробнее
В данном разделе Вы можете ознакомиться с текущими вакансиями и/или разместить своё резюмеПодробнее
Настоящее постановление утратило силу в соответствии с постановлением Кабинета Министров Республики Узбекистан от 12 мая 2017 года № 284 «О мерах по дальнейшему совершенствованию порядка лицензирования фармацевтической деятельности».
Во исполнение постановления Президента Республики Узбекистан от 7 апреля 2010 года № ПП-1319 «О мерах по упорядочению лицензирования фармацевтической и медицинской деятельности» Кабинет Министров постановляет:
Во исполнение постановления Президента Республики Узбекистан от 7 апреля 2010 года № ПП-1319 «О мерах по упорядочению лицензирования фармацевтической и медицинской деятельности» Кабинет Министров постановляет:
2. Определить, что ранее выданные лицензии на право осуществления фармацевтической деятельности действуют в течение 5 лет со дня вступления в силу настоящего постановления.
3. Министерству здравоохранения Республики Узбекистан совместно с заинтересованными министерствами и ведомствами в месячный срок:
утвердить Положение о порядке проведения аттестации и присвоения квалификационных категорий медицинским и фармацевтическим работникам;
обеспечить приведение ведомственных нормативно-правовых актов в соответствие с настоящим постановлением.
абзац третий пункта 1 постановления Кабинета Министров от 31 октября 2003 г. № 477 (СП Республики Узбекистан, 2003 г., № 10, ст. 106) и приложение № 2 к нему;
пункт 28 приложения к постановлению Кабинета Министров от 22 мая 2006 г. № 92 (СП Республики Узбекистан, 2006 г., № 5, ст. 34).
5. Контроль за исполнением настоящего постановления возложить на заместителя Премьер-министра Республики Узбекистан А.Н. Арипова.
2. Лицензирование фармацевтической деятельности осуществляется Министерством здравоохранения Республики Узбекистан (далее — лицензирующий орган).
Для рассмотрения документов о выдаче лицензий, продлении их срока, подготовке заключений по ним в лицензирующем органе создается экспертная комиссия. Состав и положение об экспертной комиссии утверждается лицензирующим органом. При этом в состав экспертной комиссии в обязательном порядке включаются специалисты соответствующего профиля.
(абзац второй пункта 2 в редакции постановления Кабинета Министров Республики Узбекистан от 17 июля 2014 года № 196 — СЗ РУ, 2014 г., № 31, ст. 380)
Заседания экспертной комиссии проводятся не реже двух раз в месяц.
Заседания экспертной комиссии проводятся не реже двух раз в месяц.
3. Фармацевтическая деятельность, подлежащая лицензированию в соответствии с настоящим Положением, включает в себя следующие виды деятельности:
в) научно-исследовательская работа по созданию лекарственных средств и изделий медицинского назначения;
ж) выращивание, сбор, заготовка, фасовка и оптовая реализация лекарственного сырья растительного, животного и минерального происхождения.
4. Лицензии на осуществление видов фармацевтической деятельности, указанных в подпунктах «а»—«е» пункта 3 настоящего Положения, выдаются только юридическим лицам, при этом аптечным учреждениям выдаются лицензии только на виды деятельности, указанные в подпунктах «б» и «д».
Получение лицензии на виды фармацевтической деятельности, указанные в подпунктах «а» и «б» пункта 3 настоящего Положения, дает лицензиатам право на реализацию произведенных и изготовленных ими лекарственных средств и изделий медицинского назначения.
Получение лицензии на виды фармацевтической деятельности, указанные в пункте 3 настоящего Положения дает лицензиатам право на хранение, поставку лекарственных средств и изделий медицинского назначения и информацию о них в установленном законодательством порядке.
(пункт 4 в редакции постановления Кабинета Министров Республики Узбекистан от 17 июля 2014 года № 196 — СЗ РУ, 2014 г., № 31, ст. 380)
(пункт 4 в редакции постановления Кабинета Министров Республики Узбекистан от 17 июля 2014 года № 196 — СЗ РУ, 2014 г., № 31, ст. 380)
6. Лицензия выдается юридическим и физическим лицам сроком на пять лет. Лицензия может быть выдана на срок менее пяти лет только по заявлению соискателя лицензии.
7. Фармацевтическая деятельность может осуществляться юридическим или физическим лицом только по определенному в лицензии виду (части вида деятельности).
При наличии у лицензиата филиалов (территориально обособленных подразделений и объектов), используемых для осуществления лицензируемой деятельности, одновременно с лицензией выдаются заверенные лицензирующим органом ее копии по числу указанных филиалов (территориально обособленных подразделений и объектов) с указанием местоположения каждого из них.
(абзац второй пункта 7 заменен абзацами вторым и третьим постановлением Кабинета Министров Республики Узбекистан от 17 июля 2014 года № 196 — СЗ РУ, 2014 г., № 31, ст. 380)
71. Лицензирующий орган формирует реестр адресов и реестр работников аптечных учреждений, действие лицензии которых было прекращено вследствие выявленных нарушений законодательства (далее — реестр адресов и реестр работников), в том числе за грубое нарушение порядка ценообразования лекарственных средств и изделий медицинского назначения.
Сведения, внесенные в реестр адресов и реестр работников, исключаются из них по истечении трех лет с момента их внесения.
(пункт 71 введен постановлением Президента Республики Узбекистан от 14 февраля 2017 года № ПП-2773 — СЗ РУ, 2017 г., № 7, ст. 87)
(абзац второй пункта 7 заменен абзацами вторым и третьим постановлением Кабинета Министров Республики Узбекистан от 17 июля 2014 года № 196 — СЗ РУ, 2014 г., № 31, ст. 380)
71. Лицензирующий орган формирует реестр адресов и реестр работников аптечных учреждений, действие лицензии которых было прекращено вследствие выявленных нарушений законодательства (далее — реестр адресов и реестр работников), в том числе за грубое нарушение порядка ценообразования лекарственных средств и изделий медицинского назначения.
Сведения, внесенные в реестр адресов и реестр работников, исключаются из них по истечении трех лет с момента их внесения.
(пункт 71 введен постановлением Президента Республики Узбекистан от 14 февраля 2017 года № ПП-2773 — СЗ РУ, 2017 г., № 7, ст. 87)
осуществлять деятельность в пределах указанной в лицензии, а также по адресу (адресам) в соответствии с лицензионным соглашением;
иметь предназначенные для выполнения лицензируемой деятельности помещения, принадлежащие ему на праве собственности или ином законном основании и соответствующие санитарным правилам и нормам;
создавать условия осуществления конкретного лицензируемого вида деятельности, включая использование соответствующей материально-технической базы, оборудования, иных технических средств;
соблюдать требования нормативных документов, утвержденных Министерством здравоохранения Республики Узбекистан по производству, изготовлению и реализации лекарственных средств и изделий медицинского назначения;
При изготовлении лекарственных средств лицензиат также обязан заключить договор на проведение анализов лекарственных средств с уполномоченной контрольно-аналитической лабораторией.
(пункт 8 в редакции постановления Президента Республики Узбекистан от 14 февраля 2017 года № ПП-2773 — СЗ РУ, 2017 г., № 7, ст. 87)
(пункт 8 в редакции постановления Президента Республики Узбекистан от 14 февраля 2017 года № ПП-2773 — СЗ РУ, 2017 г., № 7, ст. 87)
9. Требования к материально-технической базе, оборудованию, иным техническим средствам и персоналу, необходимые для осуществления соответствующего вида фармацевтической деятельности, определяются Министерством здравоохранения Республики Узбекистан в установленном порядке.
(пункт 9 в редакции постановления Кабинета Министров Республики Узбекистан от 17 июля 2014 года № 196 — СЗ РУ, 2014 г., № 31, ст. 380)
(пункт 9 в редакции постановления Кабинета Министров Республики Узбекистан от 17 июля 2014 года № 196 — СЗ РУ, 2014 г., № 31, ст. 380)
10. Для получения лицензии соискатель лицензии представляет в лицензирующий орган следующие документы:
наименования и организационно-правовой формы юридического лица, места его нахождения (почтового адреса, наименования учреждения, банка и номера расчетного счета в учреждении банка) — для юридических лиц;
фамилии, имени, отчества, данных документа, удостоверяющего личность гражданина — для физических лиц;
лицензируемого вида деятельности (его части), которую юридическое или физическое лицо намерено реализовать, и срока, в течение которого будет осуществляться указанный вид деятельности (его часть);
б)
копию свидетельства о государственной регистрации юридического лица — для юридических лиц; копию свидетельства о государственной регистрации индивидуального предпринимателя — для физических лиц;
(подпункт «б» пункта 10 в редакции постановления Кабинета Министров Республики Узбекистан от 1 февраля 2012 года № 26 — СЗ РУ, 2012 г., № 6, ст. 57)
(подпункт «б» пункта 10 в редакции постановления Кабинета Министров Республики Узбекистан от 1 февраля 2012 года № 26 — СЗ РУ, 2012 г., № 6, ст. 57)
в) документ, подтверждающий внесение сбора за рассмотрение заявления о выдаче лицензии;
(подпункт «г» пункта 10 исключен постановлением Кабинета Министров Республики Узбекистан от 17 июля 2014 года № 196 — СЗ РУ, 2014 г., № 31, ст. 380)
(подпункт «г» пункта 10 исключен постановлением Кабинета Министров Республики Узбекистан от 17 июля 2014 года № 196 — СЗ РУ, 2014 г., № 31, ст. 380)
г) заключение территориальных органов санитарно-эпидемиологического надзора о соответствии требованиям санитарных норм и правил помещений, имеющихся у соискателя лицензии, для осуществления лицензируемого вида деятельности;
д) сведения о наличии материально-технической базы, оборудования, иных технических средств и персонала в соответствии с требованиями пункта 9 настоящего Положения;
(подпункт «е» пункта 10 исключен постановлением Кабинета Министров Республики Узбекистан от 17 июля 2014 года № 196 — СЗ РУ, 2014 г., № 31, ст. 380)
(подпункт «е» пункта 10 исключен постановлением Кабинета Министров Республики Узбекистан от 17 июля 2014 года № 196 — СЗ РУ, 2014 г., № 31, ст. 380)
е) заключение территориальных органов Госкомприроды о соответствии природоохранным требованиям видов фармацевтической деятельности, указанных в подпункте «а» пункта 3 настоящего Положения.
11. Требования от соискателя лицензии представления документов, не предусмотренных настоящим Положением, не допускается.
12. Документы доставляются соискателем лицензии в лицензирующий орган непосредственно либо через средства почтовой связи с уведомлением об их получении.
Документы принимаются ответственным секретарем экспертной комиссии лицензирующего органа по описи, копия которой направляется (вручается) заявителю с отметкой о дате приема документов. Не допускается отказ в приеме документов по причине отсутствия ответственного секретаря экспертной комиссии. В случае временного отсутствия ответственного секретаря экспертной комиссии его функции выполняет лицо, определяемое лицензирующим органом в установленном порядке.
13. За предоставление недостоверных или искаженных сведений соискатель лицензии несет ответственность в соответствии с законодательством Республики Узбекистан.
14. За рассмотрение заявления с соискателя лицензии взимается сбор в пятикратном размере минимальной заработной платы, установленной законодательством.
(абзац первый пункта 14 в редакции постановления Кабинета Министров Республики Узбекистан от 1 ноября 2012 года № 313 — СЗ РУ, 2012 г., № 44, ст. 507)
(абзац первый пункта 14 в редакции постановления Кабинета Министров Республики Узбекистан от 1 ноября 2012 года № 313 — СЗ РУ, 2012 г., № 44, ст. 507)
Сумма сбора за рассмотрение заявлений соискателей лицензии зачисляется на счет лицензирующего органа. В случае отказа соискателя лицензии от поданного заявления сумма уплаченного сбора возврату не подлежит.
15. Лицензирование фармацевтической деятельности осуществляется в соответствии со схемой, прилагаемой к настоящему Положению.
Решение о выдаче или об отказе в выдаче лицензии принимается в срок, не превышающий двадцати дней со дня получения заявления соискателя лицензии со всеми необходимыми документами.
(абзац второй пункта 15 в редакции постановления Кабинета Министров Республики Узбекистан от 17 июля 2014 года № 196 — СЗ РУ, 2014 г., № 31, ст. 380)
(абзац второй пункта 15 в редакции постановления Кабинета Министров Республики Узбекистан от 17 июля 2014 года № 196 — СЗ РУ, 2014 г., № 31, ст. 380)
16. Заявление соискателя лицензии со всеми необходимыми документами в день их приема вносится на рассмотрение экспертной комиссии.
Для определения соответствия соискателя лицензии установленным лицензионным требованиям и условиям экспертной комиссией проводится с выездом на место оценка соответствия условий для осуществления лицензируемого вида деятельности.
Оценка соответствия условий для осуществления лицензируемого вида деятельности с выездом на место осуществляется за счет собственных средств лицензирующего органа.
По представленным документам и итогам экспертизы составляется экспертное заключение о выдаче либо об отказе в выдаче лицензии.
Для подготовки соответствующих заключений лицензирующий орган вправе привлекать на договорной основе дополнительных экспертов.
Лицензирующий орган на основании заключения экспертной комиссии принимает решение о выдаче или об отказе в выдаче лицензии и в трехдневный срок в письменной форме уведомляет соискателя лицензии о принятом решении.
Уведомление о принятии решения на выдачу лицензии направляется (вручается) соискателю лицензии в письменной форме с указанием реквизитов банковского счета и сроков оплаты государственной пошлины.
(пункт 16 в редакции постановления Кабинета Министров Республики Узбекистан от 17 июля 2014 года № 196 — СЗ РУ, 2014 г., № 31, ст. 380)
17. Лицензия выдается в трехдневный срок при представлении соискателем лицензии документа, подтверждающего оплату государственной пошлины, и после подписания им лицензионного соглашения.
Лицензионное соглашение является документом, определяющим взаимные права и обязанности лицензирующего органа и лицензиата, и должно содержать:
наименование вида фармацевтической деятельности (ее части), на осуществление которой выдается лицензия;
фамилию, имя, отчество заведующего (руководителя) — для аптечных учреждений;
фамилию, имя, отчество ответственного персонала за прием, отпуск и хранение лекарственных средств и изделий медицинского назначения — для организаций, осуществляющих оптовую реализацию лекарственных средств и изделий медицинского назначения;
(пункт 17 дополнен абзацем шестым постановлением Кабинета Министров Республики Узбекистан от 17 июля 2014 года № 196 — СЗ РУ, 2014 г., № 31, ст. 380)
фамилию, имя, отчество ответственного персонала за прием, отпуск и хранение лекарственных средств и изделий медицинского назначения — для организаций, осуществляющих оптовую реализацию лекарственных средств и изделий медицинского назначения;
(пункт 17 дополнен абзацем шестым постановлением Кабинета Министров Республики Узбекистан от 17 июля 2014 года № 196 — СЗ РУ, 2014 г., № 31, ст. 380)
порядок контроля со стороны лицензирующего органа за выполнением требований и условий лицензионного соглашения;
В случае переоформления лицензии или открытия филиала в лицензионное соглашение вносятся изменения или дополнения, либо составляется новое лицензионное соглашение.
В случае открытия (закрытия) филиала, изменения адреса осуществления вида (части) деятельности, изменения заведующего аптечным учреждением или непосредственно ответственного персонала за прием, отпуск и хранение лекарственных средств и изделий медицинского назначения в лицензионное соглашение вносятся изменения или дополнения либо составляется новое лицензионное соглашение в порядке, предусмотренном главой V1 настоящего Положения.
(абзац четырнадцатый пункта 17 заменен абзацами четырнадцатым и пятнадцатым постановлением Кабинета Министров Республики Узбекистан от 17 июля 2014 года № 196 — СЗ РУ, 2014 г., № 31, ст. 380)
В случае открытия (закрытия) филиала, изменения адреса осуществления вида (части) деятельности, изменения заведующего аптечным учреждением или непосредственно ответственного персонала за прием, отпуск и хранение лекарственных средств и изделий медицинского назначения в лицензионное соглашение вносятся изменения или дополнения либо составляется новое лицензионное соглашение в порядке, предусмотренном главой V1 настоящего Положения.
(абзац четырнадцатый пункта 17 заменен абзацами четырнадцатым и пятнадцатым постановлением Кабинета Министров Республики Узбекистан от 17 июля 2014 года № 196 — СЗ РУ, 2014 г., № 31, ст. 380)
Лицензионное соглашение составляется в двух экземплярах — по одному экземпляру для лицензиата и лицензирующего органа.
Лицензии оформляются на специальном бланке. Бланки лицензий являются документами строгой отчетности, имеют учетную серию, номер и степень защищенности. Образец бланка лицензии утверждается лицензирующим органом в соответствии с постановлением Кабинета Министров от 20 декабря 2000 года № 488.
18. В случае, если лицензиат в течение трех месяцев с момента направления (вручения) уведомления о принятии решения на выдачу лицензии не представил лицензирующему органу документ, подтверждающий уплату государственной пошлины за выдачу лицензии, либо не подписал лицензионное соглашение, лицензирующий орган вправе принять решение об аннулировании лицензии.
19. В выдаче лицензии может быть отказано по основаниям, установленным статьей 17 Закона Республики Узбекистан «О лицензировании отдельных видов деятельности».
Соискатель лицензии имеет право обжаловать решение лицензирующего органа об отказе в выдаче лицензии, а также действия (бездействия) должностного лица лицензирующего органа в порядке, установленном законодательством.
20. В случае принятия решения об отказе в выдаче лицензии уведомление об отказе в выдаче лицензии направляется (вручается) соискателю лицензии в письменной форме с указанием причин отказа и срока, в течение которого соискатель лицензии, устранив указанные причины, может представить документы для повторного рассмотрения.
Срок, указанный в уведомлении об отказе в выдаче лицензии, должен быть соразмерным времени, необходимому для устранения недостатков.
(абзац первый пункта 20 в редакции постановления Кабинета Министров Республики Узбекистан от 1 февраля 2012 года № 26 — СЗ РУ, 2012 г., № 6, ст. 57)
(абзац первый пункта 20 в редакции постановления Кабинета Министров Республики Узбекистан от 1 февраля 2012 года № 26 — СЗ РУ, 2012 г., № 6, ст. 57)
При повторном рассмотрении документов не допускается предъявление со стороны лицензирующего органа новых замечаний, ранее не изложенных в письменной форме соискателю лицензии.
В случае устранения соискателем лицензии причин, послуживших основанием для отказа в выдаче лицензии, повторное рассмотрение документов осуществляется лицензирующим органом в срок, не превышающий десяти дней со дня получения заявления соискателя лицензии со всеми необходимыми документами.
При этом повторно представленные документы вносятся на рассмотрение экспертной комиссии в день их приема.
Экспертная комиссия в срок, не превышающий шести дней, повторно рассматривает представленные документы и готовит экспертное заключение по ним о выдаче или об отказе в выдаче лицензии.
Лицензирующий орган в четырехдневный срок на основании заключения экспертной комиссии принимает решение о выдаче или об отказе в выдаче лицензии.
За повторное рассмотрение заявлений соискателей лицензий сбор не взимается.
При повторном рассмотрении заявления соискателя лицензии не допускается отказ в выдаче лицензии по новым основаниям, ранее не указанным в уведомлении об отказе в выдаче лицензии.
Заявление, поданное по истечении срока, указанного в уведомлении об отказе в выдаче лицензии, считается вновь поданным.
(абзац седьмой пункта 20 заменен абзацами седьмым, восьмым и девятым постановлением Кабинета Министров Республики Узбекистан от 1 ноября 2012 года № 313 — СЗ РУ, 2012 г., № 44, ст. 507)
При повторном рассмотрении заявления соискателя лицензии не допускается отказ в выдаче лицензии по новым основаниям, ранее не указанным в уведомлении об отказе в выдаче лицензии.
Заявление, поданное по истечении срока, указанного в уведомлении об отказе в выдаче лицензии, считается вновь поданным.
(абзац седьмой пункта 20 заменен абзацами седьмым, восьмым и девятым постановлением Кабинета Министров Республики Узбекистан от 1 ноября 2012 года № 313 — СЗ РУ, 2012 г., № 44, ст. 507)
21.
В случае преобразования лицензиата — юридического лица, изменения его наименования или места нахождения (почтового адреса) лицензиат или его правопреемник обязан в месячный срок после прохождения перерегистрации обратиться с заявлением в лицензирующий орган о переоформлении лицензии с приложением к нему соответствующих документов, подтверждающих указанные сведения, и подлинника действующей лицензии.
(абзац первый пункта 21 в редакции постановления Кабинета Министров Республики Узбекистан от 17 июля 2014 года № 196 — СЗ РУ, 2014 г., № 31, ст. 380)
(абзац первый пункта 21 в редакции постановления Кабинета Министров Республики Узбекистан от 17 июля 2014 года № 196 — СЗ РУ, 2014 г., № 31, ст. 380)
В случае изменения фамилии, имени, отчества или места жительства лицензиата — физического лица, лицензиат обязан в месячный срок после прохождения перерегистрации обратиться с заявлением в лицензирующий орган о переоформлении лицензии с приложением к нему соответствующих документов, подтверждающих указанные сведения, и подлинника действующей лицензии.
(пункт 21 в редакции постановления Кабинета Министров Республики Узбекистан от 1 февраля 2012 года № 26 — СЗ РУ, 2012 г., № 6, ст. 57)
(пункт 21 в редакции постановления Кабинета Министров Республики Узбекистан от 1 февраля 2012 года № 26 — СЗ РУ, 2012 г., № 6, ст. 57)
22. До переоформления лицензии лицензиат осуществляет указанную в ней деятельность на основании ранее выданной лицензии.
23. Лицензирующий орган, рассмотрев представленные документы, оформляет лицензию на новом бланке с учетом вносимых изменений и выдает взамен действующей. Одновременно оформляются соответствующие изменения в лицензионном соглашении и вносятся соответствующие изменения в реестр лицензий. При этом срок действия лицензии остается прежним.
Переоформление лицензии осуществляется в течение пяти дней со дня получения лицензирующим органом заявления о переоформлении лицензии с приложением соответствующих документов.
При переоформлении лицензии взимается сбор в половинном размере суммы, уплачиваемой за рассмотрение заявления соискателя лицензии о выдаче лицензии. Сумма сбора зачисляется на счет лицензирующего органа.
24. По истечении срока действия лицензии она может быть продлена по заявлению лицензиата. Продление срока действия лицензии осуществляется в порядке, предусмотренном для получения лицензии.
Заявление о продлении срока действия лицензии должно быть подано в лицензирующий орган не позднее двух месяцев до истечения срока действия лицензии.
(пункт 24 в редакции постановления Кабинета Министров Республики Узбекистан от 17 июля 2014 года № 196 — СЗ РУ, 2014 г., № 31, ст. 380)
(пункт 24 в редакции постановления Кабинета Министров Республики Узбекистан от 17 июля 2014 года № 196 — СЗ РУ, 2014 г., № 31, ст. 380)
25. В случае утраты лицензии или ее порчи выдается дубликат. Для получения дубликата лицензиат обращается в лицензирующий орган с заявлением и документом, подтверждающим утрату лицензии, а также представляет квитанцию об уплате половины суммы сбора, предусмотренного для выдачи лицензии. Сумма сбора зачисляется на счет лицензирующего органа.
V1. Порядок внесения изменений и дополнений в лицензионное соглашение или составления нового лицензионного соглашения
251. В случае открытия (закрытия) филиала, изменения места осуществления деятельности, заведующего аптечным учреждением или персонала, непосредственно ответственного за прием, отпуск и хранение лекарственных средств и изделий медицинского назначения, лицензиат обращается в лицензирующий орган с заявлением о внесении в лицензионное соглашение изменений и дополнений либо составлении нового лицензионного соглашения.
252. К заявлению о внесении в лицензионное соглашение изменений и дополнений либо составлении нового лицензионного соглашения лицензиат прилагает следующие документы:
для открытия филиала, изменения места осуществления деятельности — документы, указанные в подпункте «д»пункта 10 настоящего Положения, копию лицензии и лицензионное соглашение;
в случае замены заведующего аптечным учреждением или непосредственно ответственного персонала за прием, отпуск и хранение лекарственных средств и изделий медицинского назначения — сведения о соответствии нового персонала требованиям, устанавливаемым Министерством здравоохранения Республики Узбекистан, и лицензионное соглашение;
в случае закрытия филиала — лицензионное соглашение и заверенную лицензирующим органом копию лицензии, выданной для осуществления деятельности филиала;
в случае сокращения разрешенных видов (частей) фармацевтической деятельности — оригинал лицензии и лицензионное соглашение;
документ, подтверждающий внесение сбора за рассмотрение заявления о переоформлении лицензионного соглашения.
Документы доставляются лицензиатом в лицензирующий орган непосредственно либо через средства почтовой связи.
253. Рассмотрение заявления о внесении в лицензионное соглашение изменений и дополнений либо составлении нового лицензионного соглашения, за исключением заявлений о закрытии филиалов или сокращении осуществляемых видов (частей) деятельности, осуществляется в порядке, предусмотренном в пунктах 15 и 16 настоящего Положения.
254. За рассмотрение заявления о внесении изменений и дополнений в лицензионное соглашение либо составлении нового лицензионного соглашения, взимается сбор в половинном размере суммы, уплачиваемой за рассмотрение заявления соискателя лицензии о выдаче лицензии. Сумма сбора зачисляется на счет лицензирующего органа. В случае отказа лицензиата от поданного заявления сумма уплаченного сбора возврату не подлежит.
За внесение изменений и дополнений в лицензионное соглашение либо составление нового лицензионного соглашения государственная пошлина не взимается.
255. Основаниями для отказа во внесении изменений и дополнений в лицензионное соглашение либо составлении нового лицензионного соглашения являются:
представление лицензиатом ненадлежащим образом оформленных документов;
наличие в документах, представленных лицензиатом, недостоверных или искаженных сведений;
несоответствие лицензиата лицензионным требованиям и условиям.
256. Отказ во внесении изменений и дополнений в лицензионное соглашение либо составлении нового лицензионного соглашения, а также повторное рассмотрение заявления лицензиата производится в порядке, предусмотренном в пункте 20 настоящего Положения.
257. При внесении изменений и дополнений в лицензионное соглашение либо составлении нового лицензионного соглашения лицензирующий орган вносит соответствующие изменения в реестр лицензий.
258. При открытии лицензиатом филиалов (территориально обособленных подразделений и объектов), используемых для осуществления лицензируемой деятельности, лицензирующим органом выдаются заверенные копии лицензий по числу указанных филиалов (территориально обособленных подразделений и объектов) с указанием места нахождения каждого из них.
(глава V1 введен постановлением Кабинета Министров Республики Узбекистан от 17 июля 2014 года № 196 — СЗ РУ, 2014 г., № 31, ст. 380)
V1. Порядок внесения изменений и дополнений в лицензионное соглашение или составления нового лицензионного соглашения
251. В случае открытия (закрытия) филиала, изменения места осуществления деятельности, заведующего аптечным учреждением или персонала, непосредственно ответственного за прием, отпуск и хранение лекарственных средств и изделий медицинского назначения, лицензиат обращается в лицензирующий орган с заявлением о внесении в лицензионное соглашение изменений и дополнений либо составлении нового лицензионного соглашения.
252. К заявлению о внесении в лицензионное соглашение изменений и дополнений либо составлении нового лицензионного соглашения лицензиат прилагает следующие документы:
для открытия филиала, изменения места осуществления деятельности — документы, указанные в подпункте «д»пункта 10 настоящего Положения, копию лицензии и лицензионное соглашение;
в случае замены заведующего аптечным учреждением или непосредственно ответственного персонала за прием, отпуск и хранение лекарственных средств и изделий медицинского назначения — сведения о соответствии нового персонала требованиям, устанавливаемым Министерством здравоохранения Республики Узбекистан, и лицензионное соглашение;
в случае закрытия филиала — лицензионное соглашение и заверенную лицензирующим органом копию лицензии, выданной для осуществления деятельности филиала;
в случае сокращения разрешенных видов (частей) фармацевтической деятельности — оригинал лицензии и лицензионное соглашение;
документ, подтверждающий внесение сбора за рассмотрение заявления о переоформлении лицензионного соглашения.
Документы доставляются лицензиатом в лицензирующий орган непосредственно либо через средства почтовой связи.
253. Рассмотрение заявления о внесении в лицензионное соглашение изменений и дополнений либо составлении нового лицензионного соглашения, за исключением заявлений о закрытии филиалов или сокращении осуществляемых видов (частей) деятельности, осуществляется в порядке, предусмотренном в пунктах 15 и 16 настоящего Положения.
254. За рассмотрение заявления о внесении изменений и дополнений в лицензионное соглашение либо составлении нового лицензионного соглашения, взимается сбор в половинном размере суммы, уплачиваемой за рассмотрение заявления соискателя лицензии о выдаче лицензии. Сумма сбора зачисляется на счет лицензирующего органа. В случае отказа лицензиата от поданного заявления сумма уплаченного сбора возврату не подлежит.
За внесение изменений и дополнений в лицензионное соглашение либо составление нового лицензионного соглашения государственная пошлина не взимается.
255. Основаниями для отказа во внесении изменений и дополнений в лицензионное соглашение либо составлении нового лицензионного соглашения являются:
представление лицензиатом ненадлежащим образом оформленных документов;
наличие в документах, представленных лицензиатом, недостоверных или искаженных сведений;
несоответствие лицензиата лицензионным требованиям и условиям.
256. Отказ во внесении изменений и дополнений в лицензионное соглашение либо составлении нового лицензионного соглашения, а также повторное рассмотрение заявления лицензиата производится в порядке, предусмотренном в пункте 20 настоящего Положения.
257. При внесении изменений и дополнений в лицензионное соглашение либо составлении нового лицензионного соглашения лицензирующий орган вносит соответствующие изменения в реестр лицензий.
258. При открытии лицензиатом филиалов (территориально обособленных подразделений и объектов), используемых для осуществления лицензируемой деятельности, лицензирующим органом выдаются заверенные копии лицензий по числу указанных филиалов (территориально обособленных подразделений и объектов) с указанием места нахождения каждого из них.
(глава V1 введен постановлением Кабинета Министров Республики Узбекистан от 17 июля 2014 года № 196 — СЗ РУ, 2014 г., № 31, ст. 380)
26. Контроль за соблюдением требований лицензионного соглашения осуществляется лицензирующим органом в порядке, установленном законодательством.
проводить в установленном порядке плановые проверки соблюдения лицензиатом лицензионных требований и условий;
проводить в установленном порядке внеплановые проверки соблюдения лицензиатом лицензионных требований и условий при наличии фактов, свидетельствующих об их нарушениях лицензиатом;
составлять на основании результатов проверок акты (справки) с указанием конкретных нарушений лицензиатом лицензионных требований и условий;
выносить решения, обязывающие лицензиата устранить выявленные нарушения, и устанавливать сроки, в течение которых лицензиат обязан устранить выявленные нарушения;
в порядке, установленном законодательством, выносить решения или обращаться в суд о приостановлении, прекращении либо аннулировании лицензий;
в установленном порядке направлять в налоговые органы материалы о выявленных фактах осуществления хозяйствующими субъектами фармацевтической деятельности без лицензии для принятия предусмотренных законодательством мер.
28. При проверке соблюдения лицензионных требований и условий проверяющими работниками лицензирующего органа составляется акт в двух экземплярах, один из которых передается лицензиату, второй экземпляр остается у лицензирующего органа.
29. Приостановление и прекращение действия лицензии, ее аннулирование производится в случаях и порядке, предусмотренных статьями 22—24 Закона Республики Узбекистан «О лицензировании отдельных видов деятельности».
Решение лицензирующего органа о приостановлении и прекращении действия лицензии, ее аннулировании может быть обжаловано в суд. В случае признания судом необоснованности решения лицензирующего органа, лицензирующий орган несет перед лицензиатом ответственность в размере понесенного им ущерба.
30.
Лицензирующий орган ведет реестр лицензий.
(пункт 30 в редакции постановления Кабинета Министров Республики Узбекистан от 17 июля 2014 года № 196 — СЗ РУ, 2014 г., № 31, ст. 380)
(пункт 30 в редакции постановления Кабинета Министров Республики Узбекистан от 17 июля 2014 года № 196 — СЗ РУ, 2014 г., № 31, ст. 380)
31.
В реестре лицензий должны быть указаны:
(абзац первый пункта 31 в редакции постановления Кабинета Министров Республики Узбекистан от 17 июля 2014 года № 196 — СЗ РУ, 2014 г., № 31, ст. 380)
(абзац первый пункта 31 в редакции постановления Кабинета Министров Республики Узбекистан от 17 июля 2014 года № 196 — СЗ РУ, 2014 г., № 31, ст. 380)
для юридических лиц — название организации и идентификационный номер налогоплательщика, форму собственности, фамилию, имя, отчество руководителя организации;
для физических лиц — фамилию, имя, отчество лицензиата, его паспортные данные, домашний адрес, телефон;
е) основания и даты переоформления, продления срока действия, приостановления и возобновления действия лицензий;
Информация, содержащаяся в реестрах лицензий, размещается на веб-сайте лицензирующего органа и является открытой для ознакомления.
(абзацы двенадцатый и тринадцатый пункта 31 заменены абзацем двенадцатый в соответствии с постановлениемКабинета Министров Республики Узбекистан от 1 февраля 2012 года № 26 — СЗ РУ, 2012 г., № 6, ст. 57)
(пункт 32 утратил силу в соответствии с постановлением Кабинета Министров Республики Узбекистан от 1 февраля 2012 года № 26 — СЗ РУ, 2012 г., № 6, ст. 57)
33. За выдачу или продление срока действия лицензии на фармацевтическую деятельность уплачивается государственная пошлина в десятикратном размере минимальной заработной платы.
Схема лицензирования фармацевтической деятельности
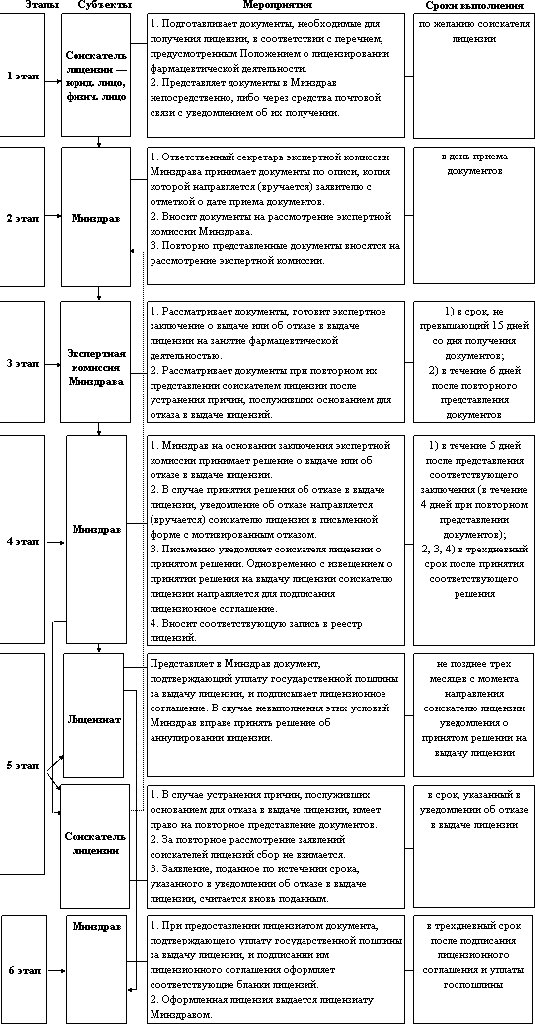
(Собрание законодательства Республики Узбекистан, 2010 г., № 18-19, ст. 142; 2012 г., № 6, ст. 57, № 44, ст. 507; 2014 г., № 31, ст. 380; 2017 г., № 7, ст. 87; 2017 г., № 14, ст. 228)
Источник: lex.uz

(Собрание законодательства Республики Узбекистан, 2010 г., № 18-19, ст. 142; 2012 г., № 6, ст. 57, № 44, ст. 507; 2014 г., № 31, ст. 380; 2017 г., № 7, ст. 87; 2017 г., № 14, ст. 228)
Источник: lex.uz
Номер документа: № 91
Дата принятия: 13.05.2010




